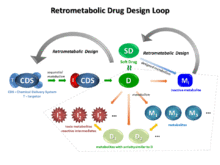
Retrometabolik ilaç tasarımı - Retrometabolic drug design
İlaç keşfi alanında , retrometabolik ilaç tasarımı , ya aktif olmayan bir kısma kadar tahmin edilebilir metabolizmayı kullanarak ya da hedefli ilaç verme yaklaşımlarını kullanarak daha güvenli ilaçların tasarımı için bir stratejidir . Retrometabolik ilaç tasarımı ifadesi Nicholas Bodor tarafından icat edildi. Yöntem, bir hedef molekülün sentezinin geriye doğru planlandığı retrosentetik analize benzer . Retrometabolik ilaç tasarımında, ilaçların metabolik reaksiyon bilgileri, etkinliği artırmak ve istenmeyen yan etkileri en aza indirmek için ilacı hedeflemek ve ortadan kaldırmak için metabolizması ve dağılımı kontrol edilebilen ana ilaçları tasarlamak için kullanılır. Bu şekilde tasarlanan yeni ilaçlar, seçici organ ve / veya terapötik bölge ilaç hedeflemesine ulaşır ve güvenli terapötik ajanlar ve güvenli çevresel kimyasallar üretir. Bu yaklaşımlar, yapı-aktivite (SAR) ve yapı-metabolizma (SMR) ilişkilerini kapsamlı bir şekilde entegre eden sistematik metodolojileri temsil eder ve iyileştirilmiş terapötik indekse (faydaya karşı yan etki oranı) sahip güvenli, lokal olarak aktif bileşikler tasarlamayı amaçlamaktadır.
Sınıflandırma
Retrometabolik ilaç tasarımı kavramı iki farklı yaklaşımı kapsar. Bir yaklaşım, istenen terapötik etkilerini uyguladıktan sonra inaktif metabolitlere öngörülebilir metabolizmaya izin vermek için özel olarak tasarlanmış bir kimyasal yapıya sahip yumuşak ilaçların (SD'ler), yeni, aktif terapötik ajanların, genellikle bir öncü bileşiğin izosterik veya izolelektronik analoglarının tasarımıdır. . Diğer yaklaşım, kimyasal dağıtım sistemlerinin (CDS'ler) tasarımıdır. CDS'ler, belirli bir organa veya bölgeye ilaç verilmesini arttırmayı amaçlayan ve aktif ilacı salmadan önce birkaç dönüşüm aşamasını gerektiren biyolojik olarak inert moleküllerdir.
Her iki retrometabolik tasarım yaklaşımı moleküler yapının kimyasal modifikasyonlarını içermesine ve her ikisi de ilaç hedeflemesini gerçekleştirmek için enzimatik reaksiyonlar gerektirmesine rağmen, SD ve CDS tasarımının prensipleri belirgin şekilde farklıdır. CDS'ler uygulandıkları gibi inaktifken ve sıralı enzimatik reaksiyonlar farklı dağılımı sağlarken ve nihayetinde aktif ilacı serbest bırakırken, SD'ler uygulandıkları gibi aktiftir ve inaktif türlere kolayca metabolize edilmek üzere tasarlanmıştır. İdeal bir durum varsayarsak, bir CDS ile ilaç bölgede bulunur ve vücudun başka hiçbir yerinde yoktur, çünkü enzimatik süreçler ilacı bu bölgelerde yok eder. CDS'ler, seçilen bir organ veya bölgede ilaç hedeflemeyi başarmak için tasarlanırken, SD'ler, ters hedefleme olarak kabul edilebilecek farklı bir dağıtım sağlamak üzere tasarlanmıştır.
Hafif ilaçlar
1970'lerin sonlarında Nicholas Bodor tarafından tanıtılmasından bu yana, yumuşak uyuşturucu kavramı hem akademik hem de endüstriyel ortamlarda önemli araştırmalar üretti. Bodor, yumuşak ilaçları, terapötik rollerini başardıktan sonra toksik olmayan kısımlara tahmin edilebilir ve kontrol edilebilir bir in vivo metabolizma ile karakterize edilen biyolojik olarak aktif, terapötik olarak yararlı kimyasal bileşikler olarak tanımladı. Piyasaya zaten ulaşmış rasyonel olarak tasarlanmış birkaç yumuşak ilaç vardır; örneğin
- esmolol (Breviblock)
- landiolol (Onoact)
- remifentanil (Ultiva)
- loteprednol etabonate (Lotemax, Alrex, Zylet)
- klevidipin (Cleviprex)
veya geç gelişme aşamasındadır ( remimazolam , budiodarone , celivarone , AZD3043 , tecafarin ). Aynı şekilde geliştirilmemiş olsalar bile yumuşak kimyasallar (ör., Malathion) veya yumuşak ilaçlar (ör., Articaine, metilfenidat) olarak kabul edilebilecek bileşikler de vardır.
Kimyasal dağıtım sistemleri
1980'lerin başında piyasaya sürülmelerinden bu yana, CDS'ler, özellikle kan-beyin bariyerini veya kan-retina bariyerini kendi başlarına geçemeyenler de dahil olmak üzere çeşitli terapötik ajanların beyin ve göz hedeflemesi için önemli araştırma çalışmaları üretti. Bu yaklaşım içinde, üç ana genel CDS sınıfı tanımlanmıştır:
- Enzimatik fizikokimyasal tabanlı (ör. Beyin hedefleme) CDS'ler: önemli ölçüde değiştirilmiş özelliklerle sonuçlanan sıralı metabolik dönüşümlerle sahaya özgü trafik özelliklerinden yararlanın
- Bölgeye özgü enzimle aktive olan (ör. Göz hedefleme) CDS'ler: öncelikle, özel olarak veya etki bölgesinde daha yüksek aktivitede bulunan belirli enzimlerden yararlanın
- Reseptör bazlı geçici ankraj tipi (örneğin, akciğer hedefleme) CDS'ler: reseptörde geçici, tersinir bağlanma yoluyla gelişmiş seçicilik ve aktivite sağlar
Bu kavram pek çok ilaç ve peptide genişletilmiştir, önemi ilk uygulamalarının ve kullanımlarının Science'da 1975, 1981 ve 1983'te yayınlanmış olmasıyla gösterilmiştir . Nöropeptitlerin hedeflenen beyin dağıtımına olan uzantısı Harvard Health tarafından dahil edilmiştir. 1992'nin en iyi 10 tıbbi ilerlemesinden biri olarak harf .
- Östradiolün beyin hedefli iletimi için E 2 -CDS (Estredox) ve
- betaksololün göz hedefli teslimi için betaxoxime
Yukarıdaki ilk örnekte, beyin hedefli CDS'ler , benzersiz özelliklerinden yararlanmak için her yerde bulunan NAD (P) H ⇌ NAD (P) + koenzim sistemi ile yakından ilişkili olan redoks bazlı bir hedefleyici parçanın sıralı bir metabolik dönüşümünü kullanır . kan-beyin bariyeri (BBB). NADH tipi ilaç konjugatının karşılık gelen NAD + - ilacına enzimatik oksidasyonundan sonra , hala aktif olmayan öncü, ilgili bileşiğin hedeflenmiş ve sürekli CNS dağıtımını sağlamak için BBB'nin arkasında "kilitlenir".
İkinci bir örnek göz özgü olarak verilmesini içerir betaxoxime , oksim türevinin betaksolol . Uygulanan, inaktif β-amino-ketoksim, yakın zamanda gözde tercihli aktivite ile tanımlanan bir enzim olan oksim hidrolaz yoluyla karşılık gelen ketona dönüştürülür ve daha sonra stereospesifik olarak alkol formuna indirgenir. GİB düşürücü aktivite, aktif -blokerleri sistemik olarak üretmeden gösterilmekte , bu da onları klasik antiglokom ajanlarının önemli bir dezavantajı olan herhangi bir kardiyovasküler aktiviteden mahrum bırakmaktadır. Bu benzersiz göz hedefleme profilinin sağladığı avantajlar nedeniyle, oksim bazlı göz hedefleyen CDS'ler, şu anda oftalmik uygulamalar için kullanılan β-blokerlerin yerini alabilir.
Tarih ve önemi
Bu retrometabolik tasarım stratejileri, ilaç tasarım sürecine metabolizma, farmakokinetik ve genel fizikokimyasal hususların erken entegrasyonu için ilk ve en önde gelen savunuculardan biri olan Nicholas Bodor tarafından tanıtıldı. Bu ilaç tasarım konseptleri, tasarım kontrollü metabolizmanın önemini kabul eder ve doğrudan aktivitenin artışına değil, aynı zamanda istenmeyen tarafı azaltır veya ortadan kaldırırken maksimum fayda sağlamak için aktivite / toksisite oranının (terapötik indeks) artışına odaklanır. Etkileri. Bu alanın önemi, konuya adanmış bir kitapta (Bodor, N .; Buchwald, P .; Retrometabolic Drug Design and Targeting , 1. baskı, Wiley & Sons, 2012) ve ayrıca tam bir bölümde gözden geçirilmiştir. Burger's Medicinal Chemistry and Drug Design , 7th ed. (2010) 150'ye yakın kimyasal yapı ve 450'den fazla referans ile. Tanıtıldığı sırada, tasarlanmış metabolizma fikri önemli bir yeniliği temsil ediyordu ve o zamanlar ilaç metabolizmasını en aza indirmeye veya tamamen ortadan kaldırmaya odaklanan ana akım düşünceye karşıydı. Bodor'un bu tasarım konseptleri üzerindeki çalışmaları, 1970'lerin sonlarında ve 1980'lerin başlarında geliştirildi ve 1990'ların ortalarında öne çıktı. Bodor tarafından tasarlanan ve patenti alınan yumuşak bir kortikosteroid olan Loteprednol etabonate, 1998'de iki oftalmik preparatın (Lotemax ve Alrex) aktif bileşeni olarak son Gıda ve İlaç İdaresi (FDA) onayını aldı, şu anda FDA tarafından tüm enflamatuarlarda kullanım için onaylanmış tek kortikosteroid. ve alerji ile ilgili oftalmik bozukluklar. Uzun süreli kullanım için güvenliği, yumuşak ilaç konseptini daha da desteklemektedir ve 2004 yılında loteprednol etabonat, bir kombinasyon ürününün (Zylet) bir parçası olarak da onaylanmıştır. Etiprednol dikloasetat gibi ikinci nesil yumuşak kortikosteroidler, rinit için burun spreyi veya astım için inhalasyon ürünleri gibi diğer olası uygulamaların tam bir yelpazesi için geliştirilmektedir.
Yumuşak ilaç kavramı hem akademik (örneğin, Aston Üniversitesi, Göteborg Üniversitesi, Okayama Üniversitesi, Uppsala Üniversitesi, İzlanda Üniversitesi, Florida Üniversitesi, Université Louis Pasteur, Yale Üniversitesi) ve endüstriyel (örneğin, AstraZeneca, DuPont, GlaxoSmithKline) araştırma çalışmalarını ateşledi. , IVAX, Janssen Pharmaceutica, Nippon Organon, Novartis, ONO Pharmaceutical, Schering AG) ayarları. Kortikosteroidlerin yanı sıra, yumuşak beta blokerler, yumuşak opioid analjetikler, yumuşak östrojenler, yumuşak beta-agonistler, yumuşak antikolinerjikler, yumuşak antimikrobiyaller, yumuşak antiaritmik ajanlar, yumuşak anjiyotensin dönüştürücü enzim (ACE) inhibitörleri, yumuşak dihidrofolat gibi çeşitli başka terapötik alanlar da araştırılmıştır. redüktaz (DHFR) inhibitörleri, yumuşak kansinörin inhibitörleri (yumuşak immünosupresanlar), yumuşak matriks metaloproteinaz (MMP) inhibitörleri, yumuşak sitokin inhibitörleri, yumuşak kanabinoidler, yumuşak Ca2 + kanal blokerleri (son incelemeye bakınız).
CDS kavramlarının tanıtılmasının ardından, dünya çapında sayısız farmasötik merkezde bu doğrultuda çalışmalar başlatıldı ve steroidler (testosteron, progestinler, estradiol, deksametazon), anti-enfektif ajanlar ( penisilinler, sülfonamidler), antiviraller (asiklovir, trifluorotimidin, ribavirin), antiretroviraller (AZT, gansiklovir), antikanser ajanlar (Lomustine, klorambusil), nörotransmiterler (dopamin, GABA), sinir büyüme faktörü (NGF) indükleyiciler, antikonvülprosanlar, stiripentol), Ca2 + antagonistleri (felodipin), MAO inhibitörleri, NSAID'ler ve nöropeptidler (triptofan, Leu-enkefalin analogları, TRH analogları, kyotorfin analogları). Yeni kimyasal yapılar bir dizi (NCE) E gibi bu ilkelerin temelinde geliştirilmiştir 2 -CDS (Estredox veya betaxoxime ileri klinik geliştirme safhalarında bulunuyor.
Nicholas Bodor tarafından geliştirilen ve düzenlenen uluslararası bir sempozyum serisi olan Retrometabolizma Temelli İlaç Tasarımı ve Hedefleme Konferansı'nda , genel retrometabolik tasarım yaklaşımları kullanılarak devam eden araştırmaların bir incelemesi iki yılda bir gerçekleştirildi . Düzenlenen her konferansın bildirileri uluslararası eczacılık dergisi Pharmazie'de yayınlandı . Geçmiş konferanslar ve yayınlanmış tutanakları şunlardır:
- Mayıs 1997, Amelia Adası, Florida; Pharmazie 52 (7) S1, 1997
- Mayıs 1999, Amelia Adası, Florida; Pharmazie 55 (3), 2000
- Mayıs 2001, Amelia Island Florida; Pharmazie 57 (2), 2002
- Mayıs 2003, Palm Coast, Florida; Pharmazie 59 (5), 2004
- Mayıs 2005, Hakone, Japonya; Pharmazie 61 (2), 2006
- Haziran 2007, Göd, Macaristan; Pharmazie 63 (3), 2008
- Mayıs 2009, Orlando, Florida; Pharmazie 65 (6), 2010
- Haziran 2011, Graz, Avusturya; Pharmazie 67 (5), 2012
- Mayıs 2013, Orlando, Florida; Pharmazie 69 (6), 2014
- Ekim 2015, Orlando, Florida.