Potasyum sülfat - Potassium sulfate
 Arkanit
|
|
|
|
| İsimler | |
|---|---|
| Diğer isimler
Potasyum sülfat
|
|
| Tanımlayıcılar | |
|
3B modeli ( JSmol )
|
|
| ChEBI | |
| ChEMBL | |
| ChemSpider | |
| ECHA Bilgi Kartı |
100.029.013 |
| E numarası | E515 (i) (asitlik düzenleyiciler, ...) |
| KEGG | |
|
PubChem Müşteri Kimliği
|
|
| RTECS numarası | |
| UNII | |
|
CompTox Kontrol Paneli ( EPA )
|
|
|
|
|
|
| Özellikleri | |
| K 2 SO 4 | |
| Molar kütle | 174.259 g / mol |
| Görünüm | Beyaz katı |
| Koku | kokusuz |
| Yoğunluk | 2,66 g / cm 3 |
| Erime noktası | 1.069 ° C (1.956 ° F; 1.342 K) |
| Kaynama noktası | 1.689 ° C (3.072 ° F; 1.962 K) |
| 111 g / L (20 ° C) 120 g / L (25 ° C) 240 g / L (100 ° C) |
|
| Çözünürlük | aseton , alkol , CS 2'de çözünmeyen gliserolde az çözünür |
| −67.0 · 10 −6 cm 3 / mol | |
|
Kırılma indisi ( n D )
|
1.495 |
| Yapısı | |
| ortorombik | |
| Tehlikeler | |
| Ana tehlikeler | Tahriş edici |
| Güvenlik Bilgi Formu | Harici MSDS |
| R cümleleri (modası geçmiş) | R22 |
| S-ibareleri (modası geçmiş) | S36 |
| Alevlenme noktası | Yanıcı değil |
| Ölümcül doz veya konsantrasyon (LD, LC): | |
|
LD 50 ( ortalama doz )
|
6600 mg / kg (oral, sıçan) |
| Bağıntılı bileşikler | |
|
Diğer anyonlar
|
Potasyum selenat Potasyum tellürat |
|
Diğer katyonlar
|
Lityum sülfat Sodyum sülfat Rubidyum sülfat Sezyum sülfat |
|
Bağıntılı bileşikler
|
Potasyum hidrojen sülfat Potasyum sülfit Potasyum bisülfit Potasyum persülfat |
|
Aksi belirtilmedikçe, veriler standart hallerinde (25 ° C [77 ° F], 100 kPa) malzemeler için verilmiştir. |
|
|
|
|
| Bilgi kutusu referansları | |
Potasyum sülfat (ABD) ya da potasyum sülfat (UK) da denilen potasyum sülfat , (SOP) Arcanite veya archaically sülfür potaş , bir inorganik bileşik , formül K 2 SO 4 , beyaz bir suda çözünebilir bir katı. Yaygın olarak kullanılan gübreler , her iki sağlayan potasyum ve kükürt .
Tarih
Potasyum sülfat (K 2 SO 4 ) 14. yüzyılın başlarından beri bilinmektedir. Glauber , Boyle ve Tachenius tarafından incelenmiştir . 17. yüzyılda, asit tuzu ile alkali tuzun bir kombinasyonu olduğu için arcanuni veya sal duplicatum olarak adlandırıldı . Aynı zamanda , onu hazırlayan ve tıbbi olarak kullanan farmasötik kimyager Christopher Glaser'den sonra vitriolic tartar ve Glaser'in tuzu veya sal polychrestum Glaseri olarak da biliniyordu .
Olarak bilinen iksir duplicatum ( "çift gizli") ya da ilacı duplicata ön modern tıp , bu (kalıntıdan elde edilmiştir kaput mortuum üretiminden arta kalan) aqua fortis (nitrik asit, HNO 3 ) gelen nitre (potasyum nitrat, Glauber prosesi yoluyla KNO 3 ) ve vitriol yağı (sülfürik asit, H 2 SO 4 ) :
- 2 KNO 3 + H 2 SO 4 → 2 HNO 3 + K 2 SO 4
Kalıntı, sıcak suda çözündürüldü, süzüldü ve buharlaştırılarak bir kütikül elde edildi. Daha sonra kristalleşmeye bırakıldı. İdrar söktürücü ve terletici olarak kullanıldı .
Chambers'ın Cyclopedia'sına göre , tarif beş yüz taler için Holstein-Gottorp Dükü Charles Frederick tarafından satın alındı . Dükün doktoru Schroder, hipokondriyak vakalardaki harika kullanımları , sürekli ve aralıklı ateşler , taş, iskorbüt ve daha fazlası hakkında harikalar yazdı .
Doğal Kaynaklar
Potasyum sülfatın mineral formu olan arkanit nispeten nadirdir. Potasyum sülfatın doğal kaynakları , Stassfurt tuzunda bol miktarda bulunan minerallerdir . Bunlar potasyum sülfat ile magnezyum , kalsiyum ve sodyum sülfatlarının birlikte kristalleşmeleridir .
İlgili mineraller:
- Kainit , KMg (SO 4 ) · Cl · 3H 2 O
- Schönite (şimdi pikromerit olarak bilinir), K 2 SO 4 · MgSO 4 · 6H 2 O
- Leonit , K 2 SO 4 · MgSO 4 · 4H 2 O
- Langbeinite K 2 , Mg 2 (SO 4 ) 3
- Aphthitalite (önceden glaserit olarak biliniyordu), K 3 Na (SO 4 ) 2
- Polihalit , K 2 SO 4 · MgSO 4 · 2CaSO 4 · 2H 2 O
Potasyum sülfat, kainit gibi bu minerallerin bazılarından ayrılabilir, çünkü karşılık gelen tuz suda daha az çözünür.
Kieserit , MgSO 4 · H 2 O, potasyum sülfat üretmek için bir potasyum klorür çözeltisi ile birleştirilebilir .
Üretim
1985 yılında, tipik olarak potasyum klorürün sülfürik asit ile reaksiyona sokulmasıyla , sodyum sülfat üretmek için Mannheim işlemine benzer şekilde yaklaşık 1,5 milyon ton üretildi . İşlem, oda sıcaklığında meydana gelen ekzotermik bir reaksiyon olan ara potasyum bisülfat oluşumunu içerir :
- KCl + H 2 SO 4 → HCl + KHSO 4
İşlemin ikinci aşaması, enerji girişi gerektiren endotermiktir:
- KCl + KHSO 4 → HCl + K 2 SO 4
Yapısı ve özellikleri
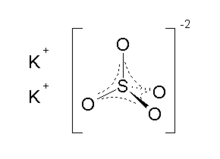
İki kristal form bilinmektedir. Ortorombik β-K 2 SO 4 yaygın formdur, ancak 583 ° C'nin üzerinde α-K 2 SO 4'e dönüşür . Bu yapılar karmaşıktır, ancak sülfat tipik dört yüzlü geometriyi benimser.
Sodyum sülfatın aksine hidrat oluşturmaz . Tuz, eşkenar dörtgen olarak sınıflandırılan çift altı kenarlı piramitler olarak kristalleşir. Şeffaftırlar, çok serttirler ve acı, tuzlu bir tada sahiptirler. Tuz suda çözünür, ancak potasyum hidroksit ( sp. Gr. 1.35) veya mutlak etanol çözeltilerinde çözünmez .
Potasyum sülfat suda ısıtıldığında ve bir beher içinde dönmeye maruz kaldığında, kristaller çökelmesine izin verildiğinde çok kollu bir spiral yapı oluşturur.
Kullanımlar
Potasyum sülfatın baskın kullanımı gübre olarak kullanılır . K 2 SO 4 , bazı mahsuller için zararlı olabilecek klorür içermez. Tütün ve bazı meyve ve sebzeleri içeren bu mahsuller için potasyum sülfat tercih edilmektedir. Daha az hassas olan mahsuller, toprak sulama suyundan klorür biriktirirse, optimum büyüme için yine de potasyum sülfat gerektirebilir.
Ham tuz ayrıca zaman zaman cam imalatında da kullanılmaktadır. Potasyum sülfat ayrıca topçu itici yüklerinde flaş düşürücü olarak kullanılır . Namlu ağzı parlamasını , parlamayı ve aşırı basıncı azaltır .
Bazen benzer alternatif bir patlama ortamı olarak kullanılan soda içinde soda patlatma zor ve benzer suda çözünür olduğu.
Potasyum sülfat, mor bir alev oluşturmak için potasyum nitrat ile kombinasyon halinde piroteknikte de kullanılabilir .
Tepkiler
Asitleştirme
Potasyum hidrojen sülfat (potasyum bisülfat olarak da bilinir), KHSO 4 , K 2 SO 4'ün sülfürik asit ile reaksiyona sokulmasıyla kolayca üretilir . 197 ° C'de (387 ° F) eriyen eşkenar dörtgen piramitleri oluşturur . 0 ° C'de (32 ° F) üç kısım suda çözünür. Çok iki gibi çözelti davranır kongenerler K 2 SO 4 ve H 2 SO 4 , birbirinden birleşmemiş yan tarafından, bu yan edildi; fazla etanol, kalan fazla asit ile normal sülfatı (az bisülfatla) çökeltir.
Kaynaşmış kuru tuzun davranışı, birkaç yüz dereceye kadar ısıtıldığında benzerdir; doğal kaynama noktasının ötesinde ısıtılan sülfürik asitle aynı şekilde silikatlar , titanatlar vb. üzerine etki eder . Bu nedenle, analitik kimyada bir parçalayıcı ajan olarak sıklıkla kullanılır. Sülfat içeren diğer tuzlar hakkında bilgi için bkz. Sülfat .



