antimon - Antimony
 | |||||||||||||||||||||
| Antimon | |||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Telaffuz | |||||||||||||||||||||
| Dış görünüş | gümüşi parlak gri | ||||||||||||||||||||
| Standart atom ağırlığı A r, std (Sb) | 121.760(1) | ||||||||||||||||||||
| Periyodik tablodaki antimon | |||||||||||||||||||||
| |||||||||||||||||||||
| Atom numarası ( Z ) | 51 | ||||||||||||||||||||
| Grup | grup 15 (pniktojenler) | ||||||||||||||||||||
| Dönem | 5. dönem | ||||||||||||||||||||
| Engellemek | p-blok | ||||||||||||||||||||
| Elektron konfigürasyonu | [ Kr ] 4d 10 5s 2 5p 3 | ||||||||||||||||||||
| Kabuk başına elektron | 2, 8, 18, 18, 5 | ||||||||||||||||||||
| Fiziki ozellikleri | |||||||||||||||||||||
| Faz de STP | sağlam | ||||||||||||||||||||
| Erime noktası | 903,78 K (630,63 °C, 1167,13 °F) | ||||||||||||||||||||
| Kaynama noktası | 1908 K (1635 °C, 2975 °F) | ||||||||||||||||||||
| Yoğunluk ( rt yakın ) | 6.697 g / cc 3. | ||||||||||||||||||||
| sıvı olduğunda ( mp'de ) | 6.53 g / cc 3. | ||||||||||||||||||||
| Füzyon ısısı | 19,79 kJ/mol | ||||||||||||||||||||
| Buharlaşma ısısı | 193.43 kJ/mol | ||||||||||||||||||||
| Molar ısı kapasitesi | 25.23 J/(mol·K) | ||||||||||||||||||||
Buhar basıncı
| |||||||||||||||||||||
| atomik özellikler | |||||||||||||||||||||
| oksidasyon durumları | -3 , -2, -1, 0, +1, +2, +3 , +4, +5 ( amfoterik oksit) | ||||||||||||||||||||
| elektronegatiflik | Pauling ölçeği: 2.05 | ||||||||||||||||||||
| iyonlaşma enerjileri | |||||||||||||||||||||
| atom yarıçapı | ampirik: 140 pm | ||||||||||||||||||||
| kovalent yarıçap | 139±5 pm | ||||||||||||||||||||
| Van der Waals yarıçapı | 206 pm | ||||||||||||||||||||
| Spektral antimon çizgileri | |||||||||||||||||||||
| Diğer özellikler | |||||||||||||||||||||
| Doğal oluşum | ilkel | ||||||||||||||||||||
| Kristal yapı | romboedrik | ||||||||||||||||||||
| Ses hızı ince çubuk | 3420 m/s (20 °C'de) | ||||||||||||||||||||
| Termal Genleşme | 11 µm/(m⋅K) (25 °C'de) | ||||||||||||||||||||
| Termal iletkenlik | 24,4 W/(m⋅K) | ||||||||||||||||||||
| elektrik direnci | 417 nΩ⋅m (20 °C'de) | ||||||||||||||||||||
| Manyetik sıralama | diamanyetik | ||||||||||||||||||||
| Molar manyetik duyarlılık | -99,0 x 10 -6 cm 3 / mol | ||||||||||||||||||||
| Gencin modülü | 55 GPa | ||||||||||||||||||||
| Kayma modülü | 20 GPa | ||||||||||||||||||||
| toplu modül | 42 GPa | ||||||||||||||||||||
| Mohs sertliği | 3.0 | ||||||||||||||||||||
| Brinell sertliği | 294–384 MPa | ||||||||||||||||||||
| CAS numarası | 7440-36-0 | ||||||||||||||||||||
| Tarih | |||||||||||||||||||||
| keşif | Arap simyacılar (MS 815'ten önce) | ||||||||||||||||||||
| Sembol | "Sb": Latince stibium'dan ' stibnite ' | ||||||||||||||||||||
| Antimonun ana izotopları | |||||||||||||||||||||
| |||||||||||||||||||||
Antimon a, kimyasal element ile sembolü Sb (adlı Latince : stibium ) ve atom numarası 51 bir parlak gri metaloidi , esas olarak doğada bulunan sülfid mineral antimonit (Sb 2 S 3 ). Antimon bileşikleri eski zamanlardan beri bilinmektedir ve genellikle Arapça kohl adıyla bilinen ilaç ve kozmetik olarak kullanılmak üzere toz haline getirilmiştir . Metalik antimon da biliniyordu, ancak keşfinden sonra yanlışlıkla kurşun olarak tanımlandı . Batı'da metalin bilinen en eski tanımı 1540 yılında Vannoccio Biringuccio tarafından yazılmıştır .
Çin en çok üretim gelen ile antimon ve bileşiklerin büyük üreticisi olduğunu Xikuangshan Mine içinde Hunan . Antimonun rafine edilmesi için endüstriyel yöntemler, kavurma ve karbon ile indirgeme veya stibnitin demir ile doğrudan indirgenmesidir .
Metalik antimon için en büyük uygulamalar kurşun ve kalay içeren bir alaşım ve kurşun-asit pillerdeki kurşun antimon plakalarıdır . Antimonlu kurşun ve kalay alaşımları, lehimler , mermiler ve kaymalı yataklar için geliştirilmiş özelliklere sahiptir . Antimon bileşikleri, birçok ticari ve yerli üründe bulunan klor ve brom içeren yangın geciktiriciler için öne çıkan katkı maddeleridir. Ortaya çıkan bir uygulama, mikroelektronikte antimon kullanımıdır .
özellikleri
Özellikler



Antimon, pnictogens adı verilen elementlerden biri olan periyodik tablonun 15. grubunun bir üyesidir ve 2.05 elektronegatifliğe sahiptir . Periyodik trendlere uygun olarak, daha elektronegatif olduğundan kalay veya bizmut ve daha az elektronegatif tellür veya arsenik . Antimon, oda sıcaklığında havada stabildir, ancak ısıtıldığında oksijenle reaksiyona girerek antimon trioksit , Sb 2 O 3 üretir .
Antimon, sert nesneler yapmak için çok yumuşak olan Mohs ölçeği sertliği 3 olan gümüşi, parlak gri bir metaloiddir . 1931'de Çin'in Guizhou eyaletinde antimon madeni paralar basıldı ; dayanıklılık zayıftı ve kısa süre sonra darphane durduruldu. Antimon asitlerin saldırılarına karşı dayanıklıdır.
Antimonun dört allotropu bilinmektedir: kararlı bir metalik form ve üç yarı kararlı form (patlayıcı, siyah ve sarı). Elementel antimon kırılgan , gümüş-beyaz, parlak bir metaloiddir. Yavaşça soğutulduğunda, erimiş antimon , arsenik gri allotropu ile izomorfik olan trigonal bir hücrede kristalleşir . Antimon triklorürün elektrolizinden nadir bir patlayıcı antimon formu oluşturulabilir . Keskin bir aletle çizildiğinde, ekzotermik bir reaksiyon meydana gelir ve metalik antimon formları olarak beyaz dumanlar çıkar; havanda bir havaneli ile ovulduğunda güçlü bir patlama meydana gelir. Antimon buharının hızlı soğuması ile siyah antimon oluşur. Kırmızı fosfor ve siyah arsenik ile aynı kristal yapıya sahiptir ; havada oksitlenir ve kendiliğinden tutuşabilir. 100 °C'de yavaş yavaş kararlı forma dönüşür. Antimonun sarı allotropu en kararsız olanıdır; sadece -90 °C'de stibinin (SbH 3 ) oksidasyonu ile üretilmiştir . Bu sıcaklığın üzerinde ve ortam ışığında, bu yarı kararlı allotrop, daha kararlı siyah allotropa dönüşür.
Elementel antimon , katmanları kaynaşmış, karıştırılmış, altı üyeli halkalardan oluşan katmanlı bir yapıya sahiptir ( uzay grubu R 3 m No. 166). En yakın ve en yakın komşular, her bir çift katmandaki üç atom, bir sonraki üç atomdan biraz daha yakın olan, düzensiz bir oktahedral kompleks oluşturur. 6.697 g / cc bir yüksek yoğunluklu Bu nispeten yakın ambalaj uçları 3 , düşük sertlik ve antimon kırılganlığı tabakalar hat arasında, ancak zayıf bağ.
izotoplar
Antimon iki sabit sahip izotopları : 121 57.36% doğal bir bolluk ile Sb ve 123 42.64% doğal bir bolluk ile Sb. Ayrıca 35 radyoizotopu vardır ve bunların en uzun ömürlüsü 125 Sb ve yarılanma ömrü 2,75 yıldır. Ek olarak, 29 yarı kararlı durum karakterize edilmiştir. Bunların en kararlısı 120m1 Sb olup, yarılanma ömrü 5.76 gündür. Kararlı 123 Sb'den daha hafif olan izotoplar, bazı istisnalar dışında, β + bozunması ile bozunma eğilimindedir ve daha ağır olanlar, β - bozunması ile bozunma eğilimindedir .
oluşum

Antimon bolluğu Toprak kabuğunda 0.2 ila 0.5 olduğu tahmin edilmektedir milyonda bir parça ile karşılaştırılabilir, talyum 0.07 ppm'de milyonda 0.5 birim ve gümüş. Bu element bol olmasa da 100'den fazla mineral türünde bulunur. Antimon bazen doğal olarak bulunur (örneğin Antimon Zirvesi'nde ), ancak daha sıklıkla baskın cevher minerali olan sülfid stibnitte (Sb 2 S 3 ) bulunur .
Bileşikler
Antimon bileşikleri genellikle oksidasyon durumlarına göre sınıflandırılır: Sb(III) ve Sb(V). +5 oksidasyon durumu daha kararlıdır.
Oksitler ve hidroksitler
Antimon havada yandığında antimon trioksit oluşur. Gaz fazında, bileşiğin molekülü Sb'dir.
4Ö
6, ancak yoğunlaşma üzerine polimerize olur. Antimon pentoksit ( Sb
4Ö
10) sadece konsantre nitrik asit ile oksidasyon ile oluşturulabilir . Antimon ayrıca karışık değerlikli bir oksit, antimon tetroksit oluşturur ( Sb
2Ö
4), hem Sb(III) hem de Sb(V) içerir. Fosfor ve arsenik oksitlerinden farklı olarak , bu oksitler amfoteriktir , iyi tanımlanmış oksoasitler oluşturmazlar ve antimon tuzları oluşturmak için asitlerle reaksiyona girerler .
Antimon asit Sb(OH)
3bilinmemektedir, ancak eşlenik baz sodyum antimonit ( [Na
3SbO
3]
4) sodyum oksit ve Sb'nin kaynaşması üzerine oluşur
4Ö
6. Geçiş metali antimonitleri de bilinmektedir. Antimonik asit sadece hidrat HSb(OH) olarak bulunur
6, antimonat anyonu Sb(OH) olarak tuzlar oluşturur-
6. Bu anyon içeren bir çözelti kurutulduğunda, çökelti karışık oksitler içerir.
Birçok antimon cevheri, stibnit ( Sb
2S
3), pirargirit ( Ag
3SBS
3), zinkenit , jamesonit ve boulangerit . Antimon pentasülfid olan stoikiometrik olmayan ve +3 antimon özellikleri oksitlenme durumu ve S-S bağlarını içerir. Çeşitli thioantimonides gibi, bilinmektedir [Sb
6S
10]2–
ve [Şb
8S
13]2–
.
Halideler
Antimon iki dizi halojenür oluşturur : SbX
3ve SbX
5. trihalojenürler bir numunesi
3, SbCl
3, SbBr
3, ve Sbi
3hepsi trigonal piramidal moleküler geometriye sahip moleküler bileşiklerdir .
triflorür SbF
3Sb reaksiyonu ile hazırlanır
2Ö
3ile HF :
-
Sb
2Ö
3+ 6 HF → 2 SbF
3+ 3 Saat
2Ö
Bu bir Lewis asiti ve hali hazırda kompleks anyonlar oluşturmak için florür iyonları kabul SbF-
4ve SbF2−
5. erimiş SbF
3zayıf bir elektrik iletkenidir . triklorür SbCl
3Sb'nin çözülmesiyle hazırlanır
2S
3içinde hidroklorik asit :
-
Sb
2S
3+ 6 HCl → 2 SbCl
3+ 3 Saat
2S
pentahalidler SbF
5ve SbCl
5sahip köşeli bipyramidal moleküler geometri , gaz fazında, fakat sıvı fazda SBF
5bir polimer , oysa SBCL
5monomeriktir. SBF
5yapmak için kullanılan güçlü bir Lewis asidi olan superacid floroantimonik asit ( "H 2 SbF 7 ").
Oksihalidler , arsenik ve fosfordan ziyade antimon için daha yaygındır. Antimon trioksit konsantre asitte çözünür ve SbOCl ve (SbO) gibi oksoantimonil bileşikleri oluşturur.
2BU YÜZDEN
4.
Antimonitler, hidritler ve organoantimon bileşikleri
Bu sınıftaki bileşikler genellikle Sb 3− 'nin türevleri olarak tanımlanır . Antimon , indiyum antimonit (InSb) ve gümüş antimonid ( Ag ) gibi metallerle antimonitler oluşturur.
3Sb ). Na 3 Sb ve Zn 3 Sb 2 gibi alkali metal ve çinko antimonitler daha reaktiftir. Bu antimonidlerin asitle muamele edilmesi , son derece dengesiz gaz stibinini , SbH'yi üretir.
3:
-
Sb3–
+ 3 Saat+
→ SbH
3
Sb tedavi edilerek de stibin üretilebilir.3+
sodyum borohidrit gibi hidrit reaktifleri ile tuzlar . Stibin, oda sıcaklığında kendiliğinden ayrışır. Stibinin pozitif bir oluşum ısısı olduğundan , termodinamik olarak kararsızdır ve bu nedenle antimon hidrojen ile doğrudan reaksiyona girmez .
Organoantimon bileşikleri tipik olarak antimon halojenürlerin Grignard reaktifleri ile alkillenmesiyle hazırlanır . Karışık kloro-organik türevler, anyonlar ve katyonlar dahil olmak üzere hem Sb(III) hem de Sb(V) merkezleri ile çok çeşitli bileşikler bilinmektedir. Örnekler Sb (Cı dahil 6 H 5 ) 3 ( triphenylstibine ), Sb 2 (Cı- 6 , H 5 ) 4 (bir Sb Sb bağı) ve siklik [Sb (Cı- 6 , H 5 )] n . Pentacoordinated organoantimony bileşikler örnek olarak; Sb (Cı olmak yaygındır 6 H 5 ) 5 ve birkaç ilgili halojenürler.
Tarih
Antimon (III) sülfid , Sb 2 S 3 , tanındı hanedan öncesi Mısır göz kozmetik (şekilde sürme gibi erken yaklaşık olarak) 3100 BC , kozmetik palet icat edilmiştir.
Bir artefakt, bulunmuştur yaklaşık 3000 MÖ antimon uzanan yapılmış bir vazo parçası olduğu söylenen Telloh , Chaldea'lı (bugünkü parçası Irak ) ve 2500 yılına 2200 yılları arasında antimon uzanan kaplama bir bakır amacı olmuştur Mısır'da bulundu . Austen, 1892'de Herbert Gladstone tarafından yapılan bir konferansta , "günümüzde sadece antimonu son derece kırılgan ve kristalli bir metal olarak biliyoruz, bu da kullanışlı bir vazoya zar zor şekillendirilebiliyor ve bu nedenle bu olağanüstü 'buluş' (artifact) yukarıda bahsedilen) antimonu dövülebilir hale getirmenin kayıp sanatını temsil etmelidir."
İngiliz arkeolog Roger Moorey , eserin gerçekten bir vazo olduğuna ikna olmadı ve Selimkhanov'un Tello nesnesi (1975'te yayınlandı) analizinden sonra "metali Transkafkasya doğal antimonuyla (yani doğal metal) ilişkilendirmeye çalıştığını" ve " Transkafkasya'dan gelen antimon nesnelerin hepsi küçük kişisel süs eşyalarıdır." Bu, "antimonu dövülebilir kılma" sanatının kayıp olduğuna dair kanıtları zayıflatıyor.
Romalı bilgin Yaşlı Pliny, Natural History adlı eserinde tıbbi amaçlar için antimon sülfürü hazırlamanın çeşitli yollarını tanımladı . Yaşlı Pliny ayrıca "erkek" ve "dişi" antimon formları arasında bir ayrım yaptı; erkek formu muhtemelen sülfür iken, daha üstün, daha ağır ve daha az kırılgan olan dişi formunun doğal metalik antimon olduğundan şüphelenilmektedir.
Yunan doğa bilimci Pedanius Dioscorides , antimon sülfürün bir hava akımıyla ısıtılarak kavrulabileceğini belirtti. Bunun metalik antimon ürettiği düşünülmektedir.

Antimonun kasıtlı izolasyonu, MS 815'ten önce Cabir ibn Hayyan tarafından tanımlanmıştır . Antimon izole etmek için bir prosedür açıklaması daha sonra 1540 kitap verilmiştir De la pirotechnia tarafından Vannoccio Biringuccio tarafından daha ünlü 1556 kitap predating, Agricola , De Re Metallica . Bu bağlamda, Agricola genellikle yanlış bir şekilde metalik antimonun keşfiyle ilişkilendirilmiştir. Kitap Currus Triumphalis Antimonii 1604 yılında Almanya'da yayınlanan metalik antimon hazırlanmasını anlatan (Antimon Zafer Chariot), bir tarafından yazılmış olması amacı da yoktu Benedikten adı altında yazma, keşiş Basilius Valentinus 15. yüzyılda; otantik olsaydı, ki değil, Biringuccio'dan önce gelirdi.
Metal antimon, 1615'te Alman kimyager Andreas Libavius tarafından, erimiş bir antimon sülfür, tuz ve potasyum tartarat karışımına demir ekleyerek elde edildi . Bu prosedür, kristalli veya yıldızlı bir yüzeye sahip antimon üretti.
Flojiston teorisine karşı meydan okumaların ortaya çıkmasıyla, antimonun diğer metaller gibi sülfitleri, oksitleri ve diğer bileşikleri oluşturan bir element olduğu kabul edildi.
İçinde doğal olarak oluşan saf antimon ilk keşif yerkabuğunun tarafından tarif edilmiştir İsveçli bilim adamı ve yerel maden bölge mühendisi Anton von Swab 1783 yılında; tip-numune toplandı Sala Gümüş Madeni ait Bergslagen madencilik ilçesinde Sala , Västmanland'da , İsveç .
etimoloji
Modern diller ve geç hangi ortaçağ Latince formu, Bizans Rum antimon için isimlerini almak olduğunu antimon . Bunun kaynağı belirsizdir; tüm önerilerin biçim veya yorum açısından bazı güçlükleri vardır. Popüler etimoloji , ἀντίμοναχός gelen anti-akdeniz veya Fransızca antimon , hala taraftar vardır; bu "keşiş katili" anlamına gelir ve birçok eski simyacının keşiş ve antimonun zehirli olmasıyla açıklanır . Bununla birlikte, antimonun düşük toksisitesi (aşağıya bakınız) bunu olası kılmaz.
Bir başka popüler etimoloji, varsayımsal Yunanca ἀντίμόνος antimonos kelimesidir , "yalnızlığa karşı", "metal olarak bulunmaz" veya "alaşımsız bulunmaz" olarak açıklanmıştır. Lippmann , "çiçek" anlamına gelen varsayımsal bir Yunanca kelime olan ανθήμόνιον anthemonion'u tahmin etti ve kimyasal veya biyolojik çiçeklenmeyi tanımlayan ilgili Yunanca kelimelerin (ancak bu değil) birkaç örneğini verdi .
Antimonyumun ilk kullanımları arasında 1050-1100 yıllarında Afrikalı Konstantin tarafından Arapça tıbbi risalelerin tercümeleri yer alır . Çeşitli yetkililer inanmak antimon bazı Arapça formun bir scribal yolsuzluk olduğu; Meyerhof bunu itmid'den türetir ; Diğer ihtimaller arasında, athimar , metaloidine Arap adı ve bir hipotetik olarak-stimmi türetilen ya da Yunan paraleldir.
Antimonun (Sb) standart kimyasal sembolü , kısaltmayı stibium'dan türeten Jöns Jakob Berzelius'a aittir .
Antimon için eski kelimeler çoğunlukla baş anlamı ve ayrıca sahip sürme , antimon sülfit.
Mısırlılar antimon mśdmt derlerdi ; içinde hiyeroglifleri , ünlü belirsiz olmakla birlikte, kelimenin Kýpti formu (sap) ⲥⲧⲏⲙ olup. Yunanca kelime, στίμμι stimmi , muhtemelen bir kredi kelimesi Arapça veya Mısır dan STM
|
5. yüzyılın Attika trajik şairleri tarafından kullanılır . Daha sonra Yunanlılar , MS birinci yüzyılda Latince yazan Celsus ve Pliny'nin yaptığı gibi στἰβι stibi'yi de kullandılar . Pliny ayrıca stimi , larbaris , kaymaktaşı ve "çok yaygın" platyoftalmi , "geniş göz" (kozmetiğin etkisinden) adlarını verir . Daha sonra Latin yazarlar, kelimeyi Latince'ye stibium olarak uyarladılar . Maddenin Arapça kelimesi, kozmetik yerine إثمد ithmid, athmoud, othmod veya uthmod olarak görünebilir . Littré , en eski olan ilk biçimin, uyaran için bir suçlayıcı olan stimmida'dan türediğini öne sürer .
Üretme
En iyi üreticiler ve üretim hacimleri
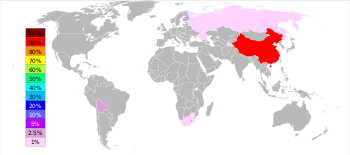
İngiliz Jeolojik Araştırmalar (BGS) 2005 yılında Çin Güney Afrika, Bolivya ve Tacikistan tarafından bir mesafede takip Dünya payının yaklaşık% 84 ile antimon üst üreticisi olduğunu bildirdi. Hunan eyaletindeki Xikuangshan Madeni , tahmini 2,1 milyon mt yatakla Çin'deki en büyük yataklara sahiptir.
2016 yılında ABD Jeolojik Araştırması'na göre Çin, toplam antimon üretiminin %76,9'unu oluştururken, onu %6,9 ile Rusya ve %6,2 ile Tacikistan takip etti.
| Ülke | Ton | % Toplam |
|---|---|---|
|
|
100.000 | 76.9 |
|
|
9.000 | 6.9 |
|
|
8.000 | 6.2 |
|
|
4.000 | 3.1 |
|
|
3.500 | 2.7 |
| En iyi 5 | 124.500 | 95.8 |
| toplam dünya | 130.000 | 100.0 |
Çin'in antimon üretiminin gelecekte, madenler ve izabe tesislerinin kirlilik kontrolünün bir parçası olarak hükümet tarafından kapatılması nedeniyle düşmesi bekleniyor. Özellikle Ocak 2015'te yürürlüğe giren çevre koruma kanunu ve revize edilen "Stanum, Antimon ve Cıva Kirleticilerinin Emisyon Standartları"nın yürürlüğe girmesi nedeniyle ekonomik üretimin önündeki engeller daha da artmaktadır. Çin'deki Ulusal İstatistik Bürosu'na göre, Eylül 2015 itibariyle Hunan eyaletindeki (Çin'deki en büyük antimon rezervine sahip eyalet) antimon üretim kapasitesinin %50'si kullanılmamıştı.
Roskill raporuna göre, Çin'de bildirilen antimon üretimi düştü ve önümüzdeki yıllarda artması pek olası değil. Çin'de yaklaşık on yıldır önemli bir antimon yatağı geliştirilmemiştir ve kalan ekonomik rezervler hızla tükenmektedir.
Roskill'e göre dünyanın en büyük antimon üreticileri aşağıda listelenmiştir:
| Ülke | Şirket | Kapasite (yılda ton) |
|---|---|---|
|
|
Hsikwangshan Parlayan Yıldız | 55.000 |
|
|
Çin Teneke Grubu | 20.000 |
|
|
Hunan Chenzhou Madencilik | 20.000 |
|
|
Shenyang Huachang Antimon | 15.000 |
|
|
GeoProMadencilik | 6.500 |
|
|
Kunduz Deresi | 6.000 |
|
|
Konsolide Murchison | 6.000 |
|
|
çeşitli | 6.000 |
|
|
zob'u aç | 5.500 |
|
|
çeşitli | 5.460 |
|
|
Mandalay Kaynakları | 2.750 |
|
|
Cengiz & Özdemir Antimuan Madenleri | 2.400 |
|
|
Kazzinç | 1.000 |
|
|
Bilinmeyen | 600 |
|
|
Kadamdzhai | 500 |
|
|
SRS | 500 |
|
|
ABD Antimonu | 70 |
Rezervler
| Ülke | Rezervler (tonlarca antimon içeriği) |
% Toplam |
|---|---|---|
|
|
950.000 | 47.81 |
|
|
350.000 | 17.61 |
|
|
310.000 | 15.60 |
|
|
140.000 | 7.05 |
|
|
60.000 | 3.02 |
|
|
50.000 | 2.52 |
|
|
27.000 | 1.36 |
| Diğer ülkeler | 100.000 | 5.03 |
| toplam dünya | 1.987.000 | 100.0 |
Üretim süreci
Cevherlerden antimon çıkarılması, cevherin kalitesine ve bileşimine bağlıdır. Çoğu antimon sülfür olarak çıkarılır; düşük dereceli cevherler köpüklü yüzdürme ile konsantre edilirken, yüksek dereceli cevherler, stibnitin eridiği ve gang minerallerinden ayrıldığı sıcaklık olan 500-600 °C'ye ısıtılır . Antimon, ham antimon sülfürden hurda demir ile indirgeme yoluyla izole edilebilir:
-
Sb
2S
3 + 3 Fe → 2 Sb + 3 FeS
Sülfür bir okside dönüştürülür; ürün daha sonra kavrulur, bazen geri kazanılan uçucu antimon(III) oksidi buharlaştırmak amacıyla. Bu malzeme genellikle doğrudan ana uygulamalar için kullanılır, safsızlıklar arsenik ve sülfürdür. Antimon oksitten bir karbotermal indirgeme ile izole edilir:
- 2 yemek kaşığı
2Ö
3+ 3 C → 4 Sb + 3 CO
2
Düşük dereceli cevherler yüksek fırınlarda indirgenirken , yüksek dereceli cevherler yankı fırınlarında indirgenir .
Tedarik riski ve kritik mineral sıralamaları
Antimon, mevcut ekonomiyi ve yaşam tarzını sürdürmek için gerekli kimyasal elementlerin veya element gruplarının tedarikine yönelik göreceli riski gösteren elementin kritikliği ile ilgili olarak Avrupa ve ABD risk listelerinde sürekli olarak üst sıralarda yer almıştır .
Avrupa'ya ve ABD'ye ithal edilen antimonun çoğu Çin'den geldiğinden, Çin üretimi tedarik için kritik önem taşıyor. Çin, çevresel kontrol standartlarını revize edip artırdıkça, antimon üretimi giderek daha fazla kısıtlanıyor. Ek olarak, Çin'in antimon ihracat kotaları son yıllarda azalmaktadır. Bu iki faktör hem Avrupa hem de ABD için arz riskini artırıyor.
Avrupa
BGS Risk Listesi 2015'e göre, antimon, nispi arz riski endeksinde (nadir toprak elementlerinden sonra) ikinci en yüksek sırada yer almaktadır. Bu, İngiliz ekonomisi ve yaşam tarzı için ekonomik değeri olan kimyasal elementler veya element grupları için şu anda ikinci en yüksek arz riskine sahip olduğunu göstermektedir. Ayrıca 2014 yılında yayınlanan bir raporda (2011'de yayınlanan ilk raporu revize eden) antimon, AB için 20 kritik hammaddeden biri olarak tanımlanmıştır. Şekil xxx'de görüldüğü gibi antimon, ekonomik önemine göre yüksek arz riskini sürdürmektedir. Antimonun %92'si Çin'den ithal edilmekte olup, bu da üretimin önemli ölçüde yüksek bir konsantrasyonudur.
Biz
ABD'de, hangi metallerin ulusun güvenliği için stratejik veya kritik olarak adlandırılması gerektiğini tanımlamaya yönelik birçok analiz yapılmıştır. Kesin tanımlar mevcut değildir ve ABD güvenliği için neyin stratejik veya kritik bir mineral oluşturduğuna dair görüşler farklıdır.
2015 yılında ABD'de antimon çıkarılmadı, metal ithal edildi. 2011-2014 döneminde Amerika'nın antimonunun %68'i Çin'den, %14'ü Hindistan'dan, %4'ü Meksika'dan ve %14'ü diğer kaynaklardan geldi. Halihazırda kamuya açık olarak bilinen bir devlet stoğu bulunmamaktadır.
ABD "Kritik ve Stratejik Maden Tedarik Zincirleri Alt Komitesi" 1996'dan 2008'e kadar 78 maden kaynağını taradı. Antimon da dahil olmak üzere küçük bir mineral alt kümesinin sürekli olarak potansiyel olarak kritik mineraller kategorisine düştüğünü tespit etti. Gelecekte, hangilerinin önemli risk ve ABD çıkarları için kritik olarak tanımlanması gerektiğini belirlemek için bulunan mineral alt kümesinin ikinci bir değerlendirmesi yapılacaktır.
Uygulamalar
Antimonun yaklaşık %60'ı alev geciktiricilerde tüketilir ve %20'si piller, kaymalı yataklar ve lehimler için alaşımlarda kullanılır.
Alev geciktiriciler
Antimon esas olarak aleve dayanıklı bileşikler için trioksit olarak kullanılır , halojen içeren polimerler hariç her zaman halojenli alev geciktiricilerle kombinasyon halinde kullanılır. Antimon trioksitin alev geciktirici etkisi, hidrojen atomları ve muhtemelen oksijen atomları ve OH radikalleri ile reaksiyona giren ve böylece yangını önleyen halojenli antimon bileşiklerinin oluşumu ile üretilir. Bu alev geciktiriciler için pazarlar arasında çocuk kıyafetleri, oyuncaklar, uçaklar ve otomobil koltuk kılıfları bulunur. Onlar da eklenir poliester reçineleri içinde fiberglas kompozit ışık uçak motoru kapakları gibi öğeler için. Reçine, harici olarak oluşturulan bir alev varlığında yanacaktır, ancak harici alev kaldırıldığında sönecektir.
Alaşımlar
Antimon , kurşun ile son derece kullanışlı bir alaşım oluşturarak sertliğini ve mekanik mukavemetini arttırır. Kurşun içeren çoğu uygulama için, alaşım metali olarak değişen miktarlarda antimon kullanılır. Olarak kurşun- asit akümülatörleri , bu ilave plaka mukavemeti ve şarj özelliklerini geliştirir. Yelkenli tekneler için, en büyük yelkenli süper yatlar için 600 libreden 200 tona kadar değişen doğrultma momenti sağlamak için kurşun omurgalar kullanılır; kurşun omurganın sertliğini ve çekme mukavemetini arttırmak için, kurşun ile hacimce %2 ila %5 arasında antimon karıştırılır. Antimon, sürtünme önleyici alaşımlarda ( Babbitt metal gibi ), mermilerde ve kurşun atışlarda , elektrik kablo kılıflarında, metal tipinde (örneğin linotip baskı makineleri için), lehimde (bazı " kurşunsuz " lehimler %5 Sb içerir), içerisinde kalay ve düşük alaşımlar sertleşme kalay imalatında içeriğine organı boru .
Diğer uygulamalar
Diğer üç uygulama, dünyanın geri kalanının neredeyse tamamını tüketiyor. Bir uygulama, polietilen tereftalat üretimi için bir stabilizatör ve katalizördür . Bir diğeri , çoğunlukla TV ekranları için camdaki mikroskobik kabarcıkları gidermek için bir inceltme maddesidir - antimon iyonları oksijenle etkileşime girerek oksijenin kabarcık oluşturma eğilimini bastırır. Üçüncü uygulama pigmentlerdir.
Antimon giderek kullanılıyor yarı iletken bir şekilde katkı maddesi olarak n-tipi silikon gofret için diyotlar , kızılötesi detektörler ve Hail etkisi cihazları. 1950'lerde, npn alaşımlı bağlantı transistörlerinin yayıcıları ve toplayıcıları, kurşun- antimon alaşımının küçük boncuklarıyla katkılandı . Orta kızılötesi dedektörler için malzeme olarak indiyum antimonid kullanılır .
Biyoloji ve tıbbın antimon için çok az kullanımı vardır. Olarak bilinen antimon içeren Bakımı antimon olarak kullanılır emetiklerin . Antimon bileşikleri, antiprotozoan ilaçlar olarak kullanılır . Potasyum antimonil tartarat veya tartar emetik, bir zamanlar 1919'dan itibaren bir anti- şistozomal ilaç olarak kullanıldı . Daha sonra prazikuantel ile değiştirildi . Antimon ve bileşikleri, geviş getiren hayvanlarda deri düzenleyici olarak antiomalin ve lityum antimon tiomalat gibi çeşitli veterinerlik preparatlarında kullanılır . Antimon, hayvanlarda keratinize dokular üzerinde besleyici veya yumuşatıcı bir etkiye sahiptir .
Gibi Antimon bazlı ilaçlar, meglumin antimoniyat da tedavisi için tercih edilen ilaçlar olarak kabul edilir layşmanyazı içinde evcil hayvan . Düşük terapötik indekslere sahip olmanın yanı sıra , ilaçlar , bazı Leishmania amastigotlarının bulunduğu kemik iliğine minimal penetrasyona sahiptir ve hastalığın tedavisi - özellikle viseral form - çok zordur. Antimon hapı olarak elemental antimon, bir zamanlar ilaç olarak kullanılmıştır. Yutma ve eliminasyondan sonra başkaları tarafından tekrar kullanılabilir.
Antimon(III) sülfür bazı güvenlik maçlarının başlarında kullanılmaktadır . Antimon sülfürler, otomotiv fren balatası malzemelerinde sürtünme katsayısını stabilize etmeye yardımcı olur. Antimon mermi, mermi izleyiciler, boya, cam sanayide kullanılan ve bir gibidir opaklaştırıcının içinde emaye . Antimon-124 ile kullanılan bir aradadır berilyum olarak nötron kaynağı ; Gama ışınları antimon-124 tarafından yayılan başlatmak photodisintegration berilyum. Yayılan nötronların ortalama enerjisi 24 keV'dir. Başlangıç nötron kaynaklarında doğal antimon kullanılmaktadır .
Tarihsel olarak, ezilmiş antimondan ( kohl ) elde edilen toz , eskilerin göz enfeksiyonlarını iyileştirmeye yardımcı olduğu düşünülen metal bir çubuk ve kişinin tükürüğü ile gözlere uygulandı. Bu uygulama hala Yemen'de ve diğer Müslüman ülkelerde görülmektedir.
Önlemler
Antimon ve bileşiklerinin insan ve çevre sağlığı üzerindeki etkileri çok farklıdır. Elementel antimon metali insan ve çevre sağlığını etkilemez. Antimon trioksitin (ve antimon tozu gibi benzer zayıf çözünür Sb(III) toz parçacıklarının) solunması zararlı olarak kabul edilir ve kansere neden olduğundan şüphelenilir. Bununla birlikte, bu etkiler yalnızca dişi sıçanlarda ve uzun süreli yüksek toz konsantrasyonlarına maruz kaldıktan sonra gözlenir. Etkilerin, antimon iyonlarına maruz kalmaya değil, akciğer klirensinin bozulmasına, akciğer aşırı yüklenmesine, iltihaplanmaya ve nihayetinde tümör oluşumuna yol açan zayıf çözünür Sb partiküllerinin solunmasına atfedildiği varsayılmaktadır (OECD, 2008). Antimon klorürler cilt için aşındırıcıdır. Antimonun etkileri arsenik ile karşılaştırılamaz; bunun nedeni arsenik ve antimon arasındaki alım, metabolizma ve atılımdaki önemli farklılıklar olabilir.
Oral absorpsiyon için, ICRP (1994), tartar emetik için %10 ve diğer tüm antimon bileşikleri için %1'lik değerler önermiştir. Metaller için dermal absorpsiyonun en fazla %1 olduğu tahmin edilmektedir (HERAG, 2007). Antimon trioksit ve diğer az çözünen Sb(III) maddelerinin (antimon tozu gibi) soluma emilimi %6,8 olarak tahmin edilirken (OECD, 2008), Sb(V) maddeleri için <%1'lik bir değer elde edilir. Antimon(V), hücrede kantitatif olarak antimon(III)'e indirgenmez ve her iki tür de aynı anda bulunur.
Antimon esas olarak insan vücudundan idrar yoluyla atılır. Antimon ve bileşikleri , kasten leishmaniasis hastalarını tedavi etmek için kullanılan bir ön ilaç olan antimon potasyum tartrat ("tartar emetik") dışında insan sağlığı üzerinde akut etkilere neden olmaz .
Antimon tozuyla uzun süreli cilt teması dermatite neden olabilir. Ancak, gözlemlenen deri döküntülerinin maddeye özgü olmadığı, büyük olasılıkla ter kanallarının fiziksel olarak tıkanmasından kaynaklandığı Avrupa Birliği düzeyinde kabul edilmiştir (ECHA/PR/09/09, Helsinki, 6 Temmuz 2009). Antimon tozu havada dağıldığında da patlayıcı olabilir; dökme katı haldeyken yanıcı değildir.
Antimon, güçlü asitler, halojenli asitler ve oksitleyicilerle uyumsuzdur; yeni oluşan hidrojene maruz kaldığında stibin (SbH 3 ) oluşturabilir.
8 saatlik zaman ağırlıklı (TWA) ortalama 0.5 mg / m ayarlanır 3 ile Devlet Endüstriyel Sağlık Uzmanları Amerika Konferansı tarafından Mesleki Güvenlik ve Sağlık Dairesi yasal olarak (OSHA) izin verilen kalma sınırı yerinde (PEL) . Mesleki Güvenlik ve Sağlık Ulusal Enstitüsü (NIOSH) bir belirledi tavsiye edilen sınır değerli 0.5 mg / m (İ) 3 , 8 saatlik bir TWA olarak.
Antimon bileşikleri, polietilen tereftalat (PET) üretimi için katalizör olarak kullanılır . Bazı araştırmalar, PET şişelerden sıvılara çok az antimon sızdığını bildiriyor, ancak seviyeler içme suyu yönergelerinin altında. Meyve suyu konsantrelerindeki antimon konsantrasyonları biraz daha yüksekti (44,7 µg/L'ye kadar antimon), ancak meyve suları içme suyu düzenlemeleri kapsamına girmez. İçme suyu yönergeleri şunlardır:
- Dünya Sağlık Örgütü : 20 µg/L
- Japonya: 15 µg/L
- Amerika Birleşik Devletleri Çevre Koruma Ajansı , Kanada Sağlık ve Ontario Çevre Bakanlığı: 6 µg/L
- AB ve Alman Federal Çevre Bakanlığı: 5 µg/L
Kabul edilebilir günlük alım WHO tarafından önerilen (TDI) 6 ug antimon her kg vücut ağırlığı arasındadır. Yaşam veya sağlık hemen tehlikeli antimon (IDLH) değeri, 50 mg / m 3 .
toksisite
Bazı antimon bileşikleri, özellikle antimon trioksit ve antimon potasyum tartarat gibi toksik görünmektedir. Etkiler arsenik zehirlenmesine benzer olabilir. Mesleki maruziyet solunum yolu tahrişine, pnömokonyoza , ciltte antimon lekelerine, gastrointestinal semptomlara ve kardiyak aritmilere neden olabilir. Ek olarak, antimon trioksit insanlar için potansiyel olarak kanserojendir.
Antimon ve antimon bileşiklerine inhalasyon, oral veya dermal maruziyetin ardından insanlarda ve hayvanlarda olumsuz sağlık etkileri gözlemlenmiştir. Antimon toksisitesi tipik olarak ya mesleki maruziyet nedeniyle, terapi sırasında ya da kazayla yutulmasından kaynaklanır. Antimonun vücuda deri yoluyla girip giremeyeceği açık değildir. Tükürükte düşük seviyelerde antimon bulunması da diş çürümesi ile ilişkilendirilebilir .
Ayrıca bakınız
Notlar
Referanslar
bibliyografya
- Endlich, FM (1888). "Mineral İsimlerinin Bazı İlginç Türevleri Üzerine" . Amerikan Doğabilimci . 22 (253): 21–32 [28]. doi : 10.1086/274630 . JSTOR 2451020 .
- Edmund Oscar von Lippmann (1919) Entstehung und Ausbreitung der Alchemie, teil 1. Berlin: Julius Springer (Almanca).
- Antimon için Halk Sağlığı Beyanı